Lösungen zu Check-up
Kapitel 7 Farbstoffe
________________________________________________________
Seite 128
Aufgabe 1
a Lichtabsorption: Wird ein farbiger Gegenstand mit Licht bestrahlt, so werden bestimmte Wellenlängen aus dem Spektrum aufgenommen (Lichtabsorption). Dadurch werden Elektronen der Farbstoffmoleküle auf ein höheres Energieniveau gehoben. Die für die Anregung notwendige Energie entspricht der Energie der absorbierten Wellenlänge. Die wahrgenommene Farbe ist das Resultat der Mischung der nicht vom Stoff absorbierten An teile des weißen Lichts.
Lichtemission: Abstrahlung elektromagnetischer Wellen im sichtbaren Spektrum unter Rückkehr von Elektronen aus einem angeregten Zustand in den Grundzustand. Die Anregungsenergie wird in Form von Licht emittiert. Die wahr genommene Farbe ist das Resultat des Aussendens von Licht in den Wellenlängen des sichtbaren Spektrums.
b Subtraktive Farbmischung: Teile des sichtbaren Lichts werden vom Gegenstand absorbiert. In das Auge gelangt nur der reflektierte Anteil. Die Mischfarbe wird somit bereits im betrachteten Gegenstand erzeugt. Grundfarben: Cyan, Magenta und Gelb. Werden diese drei Farben in gleicher Intensität und zu gleichen Anteilen miteinander gemischt, wird kein Licht mehr reflektiert und der Farbeindruck ist schwarz.
Additive Farbmischung: Mischung von farbigem Licht. Der Farbeindruck entsteht erst auf der Netzhaut es Auges. Grundfarben: Rot, Grün und Blau. Durch
Mischen des Lichts entstehen hellere Farbtöne. Mischt man alle drei Farben in gleicher Intensität und zu gleichen Anteilen, so ergänzen sie sich zu Weiß.
c Fluoreszenz: Emission von Licht beim Elektronenübergang aus dem angeregten Zustand in den Grundzustand unter Beibehaltung des Elektronenspins. Energie wird nicht nur als sichtbares Licht, sondern auch als Schwingungsenergie freigesetzt. Deshalb ist das emittierte Licht etwas energieärmer und damit langwelliger als das eingestrahlte Licht. Man sieht das Leuchten nur, so lange der Gegenstand mit energiereichem Licht bestrahlt wird. Phosphoreszenz: Emission von Licht auch nach dem Ausschalten der Lichtquelle. Das Elektron fällt unter Umkehrung des Elektronenspins über einen metastabilen Zustand in den Grundzustand zurück. Bei beiden Formen der Lichtemission besitzt das ausgestrahlte Licht größere Wellenlängen als das absorbierte Licht.
Aufgabe 2
Buttergelb ist ein Azofarbstoff, der im sichtbaren Spektrum (blauviolettes Licht) absorbiert. Der Farbstoff erscheint in der Komplementärfarbe Gelb. Das Chromophor besteht aus den de lokalisierten πElektronen der Benzolringe und den Stickstoffatomen der Azogruppe R–N=N–R, die die Ringe miteinander verbindet. Die tert-Aminogruppe –N(CH3)2 des Buttergelbmoleküls ist eine auxochrome Gruppe; das freie Elektronenpaar am Stickstoffatom wird in das delokalisierte Elektronensystem miteinbezogen (Elektronendonator). Sie erzeugt einen +M-Effekt, der die Elektronendichte im konjugierten π-Elektronensystem erhöht. Die Delokalisation der π-Elektronen bewirkt, dass eine geringe Anregungsenergie benötigt wird, um die Elektronen auf ein höheres Energieniveau zu heben. Beim Buttergelb genügt bereits das energiearme sichtbare Licht, um den Farbstoff gelb erscheinen zu lassen.
Aufgabe 3
a
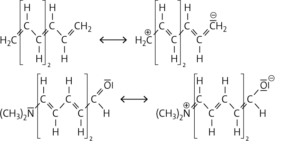
In beiden Verbindungen besitzen die Moleküle vier konjugierte Doppelbindungen. Die mesomeren Grenzstrukturen von Verbindung 1, das Polyen H–(CH=CH)4–H, zeigen, dass eine ungünstige Ladungstrennung an den Kohlenstoffatomen auftritt. Die Anregungsenergie ist dabei so hoch, dass die Absorption nur bei sehr kurzen Wellenlängen im UV-Bereich erfolgt. Verbindung 1 ist da her farblos. [Erst Polyenmoleküle mit 9 oder mehr konjugierten Doppelbindungen erscheinen farbig.]
Das Molekül von Verbindung 2 (CH3–)2N–(CH=CH)4–CHO besitzt zusätzlich zum gleichen π-Elektronensystem wie Verbindung 1 noch eine Aldehyd-Gruppe und eine tertAminogruppe. Die Aldehydgruppe ist eine antiauxochrome Gruppe mit einem −M-Effekt (Elektronenakzeptor). Die tert-Aminogruppe ist eine auxochrome Gruppe mit einem +M-Effekt (Elektronendonator). Beide Gruppen sind Bestandteil des Chromophors von Molekül 2 und vergrößern das π-Elektronensystem gegenüber der Verbindung 1, sodass die Energie zur Anregung von π-Elektronen gesenkt und Licht größerer Wellenlänge absorbiert wird. Es tritt eine bathochrome Verschiebung auf.
b
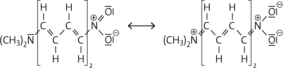
Die mesomeren Grenzstrukturen von (CH3–)2N–(CH=CH)4–NO2 zeigen, dass an der Nitrogruppe mehrere Formalladungen auftreten, die energetisch sehr ungünstig und unwahrscheinlich sind. Im Vergleich zum Ausgangsmolekül (CH3–)2N–(CH=CH)4–CHO kommt es deshalb bei (CH3–)2N–(CH=CH)4–NO2 durch den Aus tausch der antiauxochromen Gruppe zu einer hypsochromen Verschiebung (Farberhöhung).
Aufgabe 4
Ein im Tageslicht blau erscheinender Gegenstand hat sein Absorptionsmaximum im gelben Bereich des sichtbaren Lichts. In das Auge gelangt nur noch ein Teilspektrum des weißen Lichts. Die Komplementärfarbe zum absorbierten gelben Licht ist die Farbe, die vom Auge wahrgenommen wird, also Blau. Das gelbe Licht der Natriumdampflampe wird vom Gegenstand vollständig absorbiert. Es kann daher kein Licht einer anderen Wellenlänge reflektiert werden: Der Gegenstand erscheint schwarz.
Aufgabe 5
a Direktfarbstoff: wasserlöslicher Farbstoff, der beim Färben direkt aus der Färbeflotte auf die Faser zieht.
Substantive Farbstoffmoleküle lagern sich in die Hohlräume zwischen den Fasern und werden dort durch Van-der-Waals-Kräfte, Dipol-Dipol-Kräfte oder Wasserstoffbrücken gebunden. Kat ionische Farbstoffmoleküle enthalten Aminogruppen, die in saurer Lösung protoniert und daher positiv geladen sind; eignen sich zur Färbung von Polyacrylnitrilfasern, die negativ geladene Atomgruppen besitzen. Anionische Farbstoffmoleküle enthalten Carboxy oder Sulfonsäuregruppen. Durch Protolyse der Farbstoffmoleküle bilden sich negativ geladene Farbstoff-Anionen, die mit den protonierten Aminogruppen von Woll- und Polyamidfasern reagieren.
Leukoform: reduzierte Form eines Farbstoffs, die nicht farbig ist, weil das konjugierte π-Elektronensystem unterbrochen ist.
Carbonylfarbstoff: Farbstoffgruppe mit mindestens zwei Carbonylgruppen in ihren Molekülen, die durch ein konjugiertes πElektronensystem miteinander verbunden sind. Carbonylfarbstoffe sind besonders lichtecht und bleichen unter Lichteinwirkung kaum aus. Beispiele: Indigo und Anthrachinonfarbstoffe
b Indigo ist nicht wasserlöslich, eine direkte Färbung daher nicht möglich. Indigo gehört genau genommen zu den Pigmenten und nicht zu den Farbstoffen. Zum Färben wird Indigo durch Verküpung in alkalischer Lösung reduziert und in eine wasserlösliche, gelblichweiße Form, das Leukoindigo, gebracht. Dieses kann auf die zu färbenden Stoffe aufziehen. Durch den Sauerstoff der Luft erfolgt die Oxidation zum blauen Indigo.
Aufgabe 6
a Resorcingelb ist ein Azofarbstoff. Die Moleküle enthalten die Azogruppe R–N=N–R zwischen zwei aromatischen Resten. Ein aromatischer Rest besteht aus einem Benzolring mit zwei Hydroxygruppen in ortho- bzw. para-Stellung zur Azogruppe, ein weiterer aus einem Benzolring mit einer deprotonierten Sulfonsäuregruppe (Sulfonatgruppe) in para-Stellung zur Azogruppe.
b Reaktionsmechanismus (elektrophile Substitution) der Azokupplung:
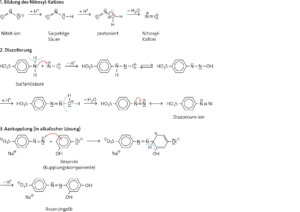
________________________________________________________
Seite 129
Anthocyane – pflanzliche Farbstoffe
Aufgabe 1
Die Moleküle der Farbstoffe Pelargonidin, Cyanidin und Delphinidin besitzen dieselbe Grundstruktur aus drei aromatischen Ringen. Bei allen drei Molekülen besteht ein ausgedehntes delokalisiertes π-Elektronensystem, das für die jeweilige Farbe verantwortlich ist. Die drei Moleküle unterscheiden sich in der Anzahl der Substituenten am rechten Ring:
– Pelargonidinmolekül: eine Hydroxygruppe (C-4-Atom)
– Cyanidinmolekül: zwei Hydroxygruppen (C-3- und C-4- Atom)
– Delphinidinmolekül: drei Hydroxygruppen (C-3-, C-4- und C-5-Atom)
Hydroxygruppen sind auxochrome Gruppen mit einem +M-Effekt. Mit zunehmender Anzahl an Hydroxygruppen wird das delokalisierte π-Elektronensystem erweitert und daher die Lichtabsorption in der Reihe Pelargonidin (Absorptionsmaximum: 506 nm), Cyanidin (Absorptions- maximum: 525 nm) und Delphinidin (Absorptionsmaximum: 540 nm) in den längerwelligen Bereich verschoben. Die durch Pelargonidin gefärbten Blütenblätter erscheinen orangerot. Jeder Gegenstand absorbiert die zu seiner Eigenfarbe komplementäre Farbe. Eine rote Blüte absorbiert aus weißem Licht die blaugrünen Farbanteile (Absorptionsmaximum des Pelargonidins: 506 nm). Die wahrgenommene Farbe ist die Komplementärfarbe zum absorbierten Licht. Blüte bzw. Farbstofflösung haben daher die Komplementärfarbe zur Farbe Blaugrün und erscheinen rot.
Die durch Cyanidin gefärbten Blütenblätter erscheinen rotviolett. Eine rotviolette Blüte absorbiert aus weißem Licht die grünen Farbanteile (Absorptionsmaximum des Cyanidins: 525 nm). Blüte und Farbstofflösung haben daher die Komplementärfarbe zur Farbe Grün und er- scheinen rotviolett.
Die durch Delphinidin gefärbten Blütenblätter erscheinen violett. Eine violette Blüte absorbiert aus weißem Licht die hellgrünen Farbanteile (Absorptionsmaximum des Delphinidins: 540 nm). Blüte und Farbstofflösung haben daher die Komplementärfarbe zur Farbe Hellgrün und erscheinen violett.
Hinweis: Die jeweilige Farbe der drei Farbstoffe aus der Gruppe der Anthocyanidine hängt auch vom pH-Wert des Zellsafts ab. Außerdem bilden die Farbstoffe Komplexe mit Metallkationen, die Farbvariationen bewirken können.
Aufgabe 2
a Das Diagramm zeigt die Absorptionsspektren von Cyanidin bei pH = 3, pH = 6 und pH = 8. Auf der x-Achse ist die Wellenlänge in Nanometern aufgetragen, auf der y-Achse die Absorption in relativen Einheiten.
Die drei Absorptionsspektren zeigen, dass Cyanidin bei den gegebenen pH-Werten zwischen 350 und 400 nm nur sehr wenig Licht absorbiert. Bei pH = 3 liegt das Absorptionsmaximum des Cyanidins bei ungefähr 525 nm; bei pH = 6 bei ungefähr 565 nm; bei pH = 8 liegt das Absorptionsmaximum bei 585 nm. Alle drei Absorptionsspektren sind Optimumskurven. Bei größeren Wellenlängen als dem jeweiligen Absorptionsmaximum sinkt die Absorption allmählich wieder auf 0 ab.
b Die wahrgenommene Farbe ist die Komplementärfarbe zum absorbierten Licht.
| Cyanidin bei pH | Absorptionsmaximum in nm | wahrgenommene Farbe |
| 3 | 525 (Grün) | Rotviolett |
| 6 | 565 (Hellgrün) | Violett |
| 8 | 585 (Gelb) | Blau |
c Mit zunehmendem pH-Wert werden mehr Hydroxygruppen deprotoniert. Die dabei entstehenden Sauerstoff-Anionen mit drei freien Elektronenpaaren besitzen einen stärkeren +M-Effekt als die Hydroxygruppe mit nur zwei freien Elektronenpaaren am Sauerstoffatom. Da das Sauerstoff-Anion ein stärkeres Auxochrom als die Hydroxygruppe ist, tritt mit steigendem pH-Wert eine bathochrome Farbverschiebung von Rotviolett über Violett zu Blau auf.
Aufgabe 3
Beim zuerst beschriebenen Färbeverfahren handelt es sich um das substantive Direktfärben, bei dem eine aus Cellulosefasern bestehende Baumwolle in heißem Rotkohlextrakt gefärbt wird. Die Moleküle der Cellulosefasern besitzen als funktionelle Gruppen ungeladene Hydroxygruppen. Beim substantiven Direktfärben lagert sich das Cyanidin aus dem Rotkohlextrakt in die Hohl- räume zwischen den Fasern ein. Das Cyanidinmolekül besitzt ebenfalls viele Hydroxygruppen und haftet nur durch zwischenmolekulare Wechselwirkungen (Van-der- Waals-Kräfte, Dipol-Dipol-Kräfte oder Wasserstoff- brücken) an den Cellulosemolekülen. Das Ergebnis dieser Färbung ist nur wenig waschecht.
Die zweite Stoffprobe aus Baumwolle wird einer Beizenfärbung unterzogen, bei dem die Stoffprobe zunächst in einer Lösung von Alaun (Kaliumaluminiumsulfat) gebeizt wird. Die so vorbehandelte Stoffprobe wird anschließend in ein Becherglas mit heißem Rotkohlextrakt gegeben. Durch das Beizen wird die Haftung des wasserlöslichen Cyanidins auf der Cellulosefaser verbessert, indem die Al3+-Ionen aus der Beize an die Cellulosemoleküle der Fasern binden und gleichzeitig eine Bindung mit Hydroxygruppen bzw. deprotonierten Hydroxygruppen der Cyanidinmoleküle eingehen. Dadurch entsteht eine wasserunlösliche Verbindung, ein Farblack, zwischen Cyanidinmolekülen, Aluminium-Ionen und Cellulosemolekülen.
Aufgabe 4
Rotkohlextrakt ist gesundheitlich unbedenklich, da er aus einer essbaren, ungiftigen Pflanze durch Auskochen gewonnen wird. Die Farbe des Cyanidins ist jedoch nicht pH-beständig – je nach pH-Wert wechselt Rotkohlextrakt die Farbe von Rot über Blau nach Grün. Daher ist Cyanidin nicht für Kleidungsstücke geeignet, die direkt auf der Haut getragen werden, weil beispielsweise Schweiß aufgrund seines pH-Werts die Farbe des mit Cyanidin gefärbten Kleidungsstücks ändern würde. Außerdem sind Pflanzenfarbstoffe wenig lichtecht und bleichen mit der Zeit aus. Eine Färbung von Kleidungsstücken mit Cyanidin ist daher zwar gesundheitlich unbedenklich, jedoch von äußerst geringem Gebrauchswert.
© Cornelsen Verlag GmbH