Abitraining Chemie Klausur Leistungskurs 6
Thema: Carmoisin – Synthese und Einsatz als Lebensmittelfarbstoff
Orientierungen zur Lösung
_______________________________________________________
Aufgabe 1: Geben Sie die Kennzeichen aromatischer Systeme an. Erläutern Sie anhand der Molekülstrukturen das unterschiedliche Verhalten von Stoff A (Naphthalin) und Stoff B (1,2,3,4,5,8-Hexahydronaphthalin) gegenüber Brom. Erläutern Sie den Ablauf der Reaktion von Stoff B und Brom in Einzelschritten.
Teil 1) die Kennzeichen aromatischer Systeme angeben:
• planares Ringsystem,
• delokalisiertes π-Elektronensystem,
• Mesomeriestabilisierung,
• Hückel-Regel (alternativ: [4n + 2] π-Elektronen)
Teil 2) anhand der Molekülstrukturen das unterschiedliche Verhalten von Stoff A (Naphthalin) und Stoff B (1,2,3,4,5,8-Hexahydronaphthalin) gegenüber Brom erläutern:
• Bei Stoff A (Naphthalin) handelt es sich um eine aromatische Verbindung mit delokalisiertem π-Elektronensystemen, die aufgrund des Energiegewinns durch Mesomerie energieärmer und stabiler ist.
• Eine elektrophile Addition von Brom an den Aromaten kann aufgrund der Mesomeriestabilisierung nicht erfolgen.
• Bei Stoff B liegen isolierte Doppelbindungen vor, die leichter elektrophil angreifbar sind; hier erfolgt bei Raumtemperatur eine elektrophile Addition der Brom-Moleküle an die Doppelbindungen.
Teil 3) den Ablauf der Reaktion von Stoff B und Brom in Einzelschritten erläutern:
Schritt 1: Annäherung eines Brom-Moleküls an die C=C-Doppelbindung mit temporärer Polarisierung der Elektronenpaarbindung, Wechselwirkung des positiv teilgeladenen Brom-Atoms und der Doppelbindung (Tradukt), heterolytische Trennung der Bindung des Brom-Moleküls und Bildung eines Bromonium-Ions (Interdukt) sowie eines Bromid-Ions.
Schritt 2: Anlagerung eines Bromid-Ions am Bromonium-Ion (Bildung einer 1,2-Dibromverbindung).
_______________________________________________________
Aufgabe 2: Geben Sie den Reaktionstyp für die der Sulfonierung von 1-Naphthol zugrundeliegenden Reaktion an. Erläutern Sie den Ablauf dieser Reaktion in Einzelschritten. Begründen Sie die Position, an der die Sulfonierung von 1-Naphthol erfolgt.
Teil 1) den Reaktionstyp für die der Sulfonierung von 1-Naphthol zugrundeliegenden Reaktion angeben:
elektrophile Substitution
Teil 2) den Ablauf dieser Reaktion in Einzelschritten erläutern:
eingehen auf:
– elektrophiler Angriff der Schwefeltrioxid-Moleküle (stark positiv teilgeladene Schwefel-Atome)
– die Bildung eines π-Komplexes und die Bildung des mesomeriestabilisierten σ-Komplexes
– Rearomatisierung
Teil 3) die Position begründen, an der die Sulfonierung von 1-Naphthol erfolgt:
eingehen auf:
– aktivierende (+M-Effekt) und in o- und p-Position dirigierende Wirkung der Hydroxygruppe
– Bevorzugung der p-Position aus sterischen Gründen
_______________________________________________________
Aufgabe 3: Entwickeln Sie unter Angabe des Reaktionstyps und der beteiligten Stoffe eine Reaktionsgleichung für die in Schritt II der Carmoisin-Synthese ablaufende Reaktion. Geben Sie begründend die bei diesem Schritt einzuhaltenden Reaktionsbedingungen an. Entwickeln Sie unter Angabe des Reaktionstyps eine Reaktionsgleichung für die in Schritt III der Carmoisin-Synthese ablaufende Reaktion.
Teil 1) unter Angabe des Reaktionstyps und der beteiligten Stoffe eine Reaktionsgleichung für die in Schritt II der Carmoisin-Synthese ablaufende Reaktion entwickeln:
Reaktionstyp: Diazotierung,
beteiligte Stoffe: 4-Aminonaphthalin-1-sulfonsäure, Natriumnitrit und Salzsäure (alternativ: salpetrige Säure oder Nitrosyl-Kationen),
Reaktionsgleichung:
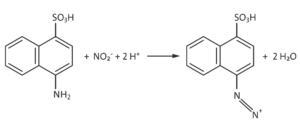
Teil 2) begründend die bei diesem Reaktionsschritt einzuhaltenden Reaktionsbedingungen angeben:
eingehen auf:
– die bei der Reaktion entstehenden Diazonium-Ionen können bei höheren Temperaturen zerfallen
– daher werden alle entsprechenden Lösungen der Schritte, in denen Diazonium-Ionen entstehen oder reagieren sollen, auf unter 5 °C gekühlt
Teil 3) unter Angabe des Reaktionstyps eine Reaktionsgleichung für die in Schritt III der Carmoisin-Synthese ablaufende Reaktion entwickeln:
Reaktionstyp: Azokupplung (alternativ: elektrophile Substitution)
Reaktionsgleichung:
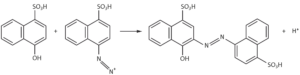
_______________________________________________________
Aufgabe 4: Erklären Sie am Beispiel von Carmoisin unter Bezug auf Tabelle 1 und das angegebene Extinktionsmaximum den Zusammenhang zwischen Lichtabsorption und Farbigkeit. Begründen Sie anhand der Molekülstruktur die Farbigkeit von Carmoisin. Erläutern Sie am Beispiel der Konzentrationsbestimmung von Carmoisin in Limonade die Grundlagen und Durchführung des fotometrischen Messverfahrens.
Teil 1) am Beispiel von Carmoisin unter Bezug auf Tabelle 1 und das angegebene Extinktionsmaximum den Zusammenhang zwischen Lichtabsorption und Farbigkeit erklären:
eingehen auf:
– die Spektralfarben des weißen Lichts
– die Anregung von Elektronen und dem Energiestufenmodell der Lichtabsorption
– das Extinktionsmaximum des angegebenen Farbstoffs
– Zusammenhang zwischen absorbierter Spektralfarbe und Eigenfarbe des Farbstoffs
(z. B.: Extinktionsmaximum von 516 nm beim Carmoisin, absorbierte Spektralfarbe Grün, Eigenfarbe Purpur)
Teil 2) anhand der Molekülstruktur die Farbigkeit von Carmoisin begründen:
eingehen auf:
– das vorliegenden ausgedehnten System konjugierter Doppelbindungen (Chromophor) + das Mesomeriemodell:
mesomere Grenzstrukturen, Delokalisation von konjugierten π-Elektronen, Einfluss von Donator-/Akzeptorgruppen, hier z. B. der Hydroxygruppe als Donatorgruppe
Teil 3) am Beispiel der Konzentrationsbestimmung von Carmoisin in Limonade die Grundlagen und Durchführung des fotometrischen Messverfahrens erläutern:
eingehen auf:
– das Lambert-Beer-Gesetz als Grundlage des fotometrischen Messverfahrens (die Extinktion eines Farbstoffes ist proportional zur Konzentration des Farbstoffes)
– Durchführung:
- Erstellung einer Kalibriergeraden (Extinktionsmessung verschiedener Carmoisinlösungen bekannter Konzentrationen, Auftragen der Extinktionswerte gegen die Konzentrationen)
- Messung einer Limonadenprobe unter gleichen Bedingungen (alle Messungen werden in Küvetten gleicher Schichtdicke bei der Wellenlänge des Extinktionsmaximums, hier 516 nm, durchgeführt)
- Ablesen der Konzentration des Farbstoffes in der Limonadenprobe direkt an der Kalibriergeraden