Abitraining Chemie Klausur Leistungskurs 5
Thema: Ballistische Schutzwesten
Orientierungen zur Lösung
_______________________________________________________
Aufgabe 1: Geben Sie die Monomere sowie den Reaktionstyp der Synthese des Polyester-Präpolymers an. Erläutern Sie unter Angabe einer Reaktionsgleichung mit Strukturformeln die Bildungsreaktion des Polyester-Präpolymers und erklären Sie, wie sich diese zugunsten einer besseren Produktausbeute steuern lässt.
Teil 1) die Monomere sowie den Reaktionstyp der Synthese des Polyester-Präpolymers angeben:
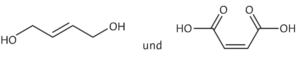
Reaktionstyp: Veresterung, Substitutions- oder Additions-Eliminierungsreaktion
(eine Bezeichnung genügt)
Teil 2) unter Angabe einer Reaktionsgleichung mit Strukturformeln die Bildungsreaktion des Polyester-Präpolymers erläutern:
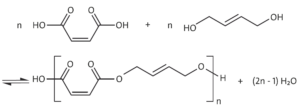
Eine Carboxygruppe des Maleinsäure-Moleküls reagiert mit einer Hydroxygruppe des Buten-1,4-diol-Moleküls unter Abspaltung eines Wasser-Moleküls und Bildung einer Estergruppe.
Teil 3) erklären, wie sich diese zugunsten einer besseren Produktausbeute steuern lässt:
• Da eine Veresterung umkehrbar ist, liegen Produkte und Edukte im chemischen Gleichgewicht vor.
• Dieses Gleichgewicht kann durch die Veränderung der Stoffmengen von Produkten und Edukten im Reaktionsgemisch beeinflusst werden.
• Dies kann zum Beispiel durch den Entzug des entstehenden Wassers geschehen.
_______________________________________________________
Aufgabe 2: Erläutern Sie unter Angabe des Reaktionstyps den Ablauf der Reaktion für die Herstellung von Cumol aus Benzol und Propen in Einzelschritten. Geben Sie begründet ein mögliches Nebenprodukt an.
Teil 1) unter Angabe der Reaktionsschritte die Herstellung von Cumol aus Benzol und Propen erläutern:
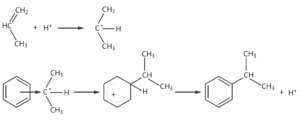
Das Wasserstoff-Ion reagiert mit dem Propen-Molekül unter Auflösung der Doppelbindung und der Bildung eines Carbenium-Ions.
Das Carbenium-Ion tritt als elektrophiles Teilchen mit den π-Elektronen des Benzol-Moleküls in Wechselwirkung (π-Komplex).
Es wird ein mesomeriestabilisierter σ-Komplex gebildet, und abschließend erfolgt die Rearomatisierung durch Protonenabspaltung.
Teil 2) begründet ein mögliches Nebenprodukt angeben:
hier gibt es zwei Möglichkeiten
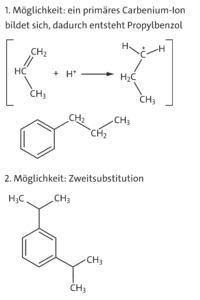
_______________________________________________________
Aufgabe 3: Erklären Sie die einzelnen Reaktionsschritte der Bildung von Poly-α-methylstyrol aus α-Methylstyrol unter Zugabe eines organischen Peroxids. Geben Sie für diese Teilschritte Reaktionsschemata an. Begründen Sie den Einsatz des Copolymers aus α-Methylstyrol und dem Polyester-Präpolymer in Schutzwesten anstelle von Poly-α-methylstyrol.
Teil 1) die einzelnen Reaktionsschritte der Bildung von Poly-α-methylstyrol aus α-Methylstyrol unter Zugabe eines organischen Peroxids erklären:
• Erzeugung von Startradikalen: Bildung von zwei Startradikalen durch homolytische Spaltung, z. B. eines organischen Peroxids (entweder durch Licht oder einen Katalysator),
• Kettenstart: Reaktion des Startradikals, z. B. mit einem α-Methylstyrol-Molekül,
• Kettenwachstum: wiederholte Reaktion des gebildeten Radikals mit einem α-Methylstyrol-Molekül,
• Kettenabbruch: Reaktion zweier Radikale zu einem Molekül, das kein Radikal ist.
Teil 2) den Einsatz des Copolymers aus α-Methylstyrol und dem Polyester-Präpolymer in Schutzwesten anstelle von Poly-α-methylstyrol begründen:
• Poly-α-methylstyrol ist als Polymer für die Matrix nicht geeignet, da es als Thermoplast schmelzen kann.
• Die zugesetzten Polyester-Präpolymer-Moleküle enthalten mehrere reaktive Doppelbindungen, sind also für die Polymerisation multifunktionale Moleküle. Über diese Moleküle erfolgt eine Vernetzung des entstehenden Polymers.
• Es bildet sich ein Duroplast, der auch bei hohen Temperaturen nicht weich wird und die Verstärkungsfaser fest einbindet.
_______________________________________________________
Aufgabe 4: Vergleichen Sie die zwischenmolekularen Wechselwirkungen im Polyaramid und im Hochleistungspolyethen mithilfe von geeigneten Strukturformelausschnitten. Erklären Sie, wie Verzweigungen in Polyethenketten die zwischenmolekularen Wechselwirkungen beeinflussen. Erläutern Sie, dass die Art der zwischenmolekularen Wechselwirkungen allein nicht ausreichend ist, um die Zugfestigkeit der Fasern einzuordnen.
Teil 1) die zwischenmolekularen Wechselwirkungen im Polyaramid und im Hochleistungspolyethen mithilfe von geeigneten Strukturformelausschnitten vergleichen:
Strukturformelausschnitt Polyaramid:
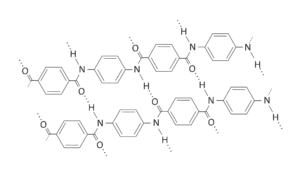
Strukturformelausschnitt Polyethen:
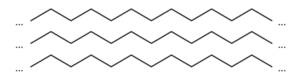
Im Polyaramid gibt es Wasserstoffbrücken zwischen den Amidgruppen und Van-der-Waals-Wechselwirkungen zwischen den aromatischen Ringen.
Beim Polyethen können sich die unverzweigten Polymerketten geordnet aneinanderlagern
und aufgrund der regelmäßigen Anordnungen leicht Van-der-Waals-Wechselwirkungen ausbilden.
Teil 2) erklären, wie Verzweigungen in Polyethenketten die zwischenmolekularen Wechselwirkungen beeinflussen:
Die Verzweigungen verhindern, dass sich die Polyethenketten parallel zueinander anordnen. Dadurch bilden sich keine hochgeordneten Zustände aus, in denen die Van-der-Waals-Kräfte besonders ausgeprägt sind.
Teil 3) erläutern, dass die Art der zwischenmolekularen Wechselwirkungen allein nicht ausreichend ist, um die Zugfestigkeit der Fasern einzuordnen:
Wasserstoffbrücken (Dipol-Dipol-Wechselwirkungen) bei polaren Strukturen wie im Polyaramid sind deutlich stärker als Van-der-Waals-Kräfte bei unpolaren Ketten wie im Polyethen. Bei gleichem Kristallisationsgrad hat deshalb das Polyaramid die höhere Zugfestigkeit. Hat das Polyethen im Vergleich zum Polyaramid einen deutlich höheren Kristallisationsgrad, so kann seine Zugfestigkeit die des Polyaramid übertreffen.