Sauber und schön: Vorbereitung
Sieh dir die Übersicht an. Sie hilft dir, die Aufgaben zu beantworten.
Löslichkeit
Feststoffe, Gase und Flüssigkeiten können sich in einer Flüssigkeit dem sogenannten Lösungsmittel lösen. Lösungsmittel sind Flüssigkeiten, die andere Stoffe feinst möglich in sich verteilen. Es handelt sich nicht immer um Wasser. Stoffe können in einem Lösungsmittel leicht oder schwer löslich sein. Die Löslichkeit wird durch die Temperatur des
Lösungsmittels beeinflusst.
Ist die maximale Menge eines Stoffes in einem Lösungsmittel gelöst, spricht man von einer gesättigten Lösung. Ist die Grenze der Löslichkeit von z. B. Salz in Wasser erreicht, bildet sich ein Bodensatz.
Dipole
Wasser ist eine Verbindung bestehend aus zwei Atomen Wasserstoff und einem Atom Sauerstoff. Aufgrund der unterschiedlichen Elektronegativitäten von Wasserstoff und Sauerstoff werden die Bindungselektronen unterschiedlich stark zu den Atomen hingezogen. Das Sauerstoff-Atom zieht die Bindungselektronen stärker an.
Dies führt zu einer Ladungsverschiebung innerhalb des Moleküls. Beim Sauerstoff-Atom bildet sich eine negative Teilladung, bei den Wasserstoff-Atomen eine positive Teilladung.
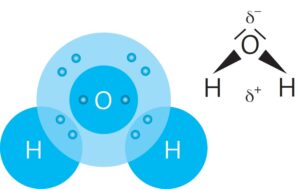
Durch den gewinkelten Bau des Wassermoleküls führen seine Teilladungen dazu, dass das gesamte Molekül zwei Pole hat: Man nennt es daher ein Dipolmolekül oder sagt auch: Die Bindungen im Wassermolekül und das ganze Molekül sind polar.
Moleküle, die verschiedene Pole ausbilden werden als Dipole bezeichnet.
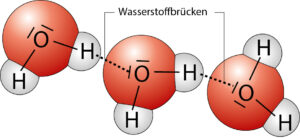
Die verschiedenen Pole benachbarter Wassermoleküle ziehen sich gegenseitig an. Diese Anziehung zwischen den Molekülen
bezeichnet man als Wasserstoffbrücke. Die Wasserstoffbrücken sorgen durch die Anziehung benachbarter Moleküle zur Seite und nach innen sowie die fehlende Anziehung nach oben für die Oberflächenspannung des Wassers. Dies ermöglicht Wasserläufern, auf dem Wasser zu laufen, als hätte es eine Haut. Auch die charakteristische runde Tropfenform kommt dadurch
zustande.
Anionen und Kationen
Atome, die Elektronen aufnehmen bzw. abgeben und folglich geladen sind, nennt man Ionen.
Ionen können positiv oder negativ geladen sein. Die positiv geladenen Ionen heißen Kationen, die negativ geladenen Ionen Anionen.
In der Formelschreibweise werden die Ladungen der Ionen als Hochzahl rechts neben dem Elementsymbol angegeben.
Beispiel für ein Kation: \( \text{Na}^{+} \)
Beispiel für ein Anion: \( \text{Cl}^{-} \)
Kannst du jetzt die Aufgaben lösen? Probiere es aus.
Illustrationen: Cornelsen/Detlef Seidensticker