Alkohole, Carbonsäuren und Kohlenhydrate: Vorbereitung
Sieh dir die Übersicht an. Sie hilft dir, die Aufgaben zu beantworten.
Oxidationen
Reaktionen, bei denen Sauerstoff beteiligt ist, nennt man Oxidationen. Die dabei entstehenden Produkte nennt man Oxide.
Beispiele:
Beispiel 1: Methan + Sauerstoff → Kohlenstoffdioxid + Wasser
Beispiel 2: Aluminiumoxid + Eisen → Eisenoxid + Aluminium
Im Beispiel 2 steckt der Sauerstoff im Aluminiumoxid und wird auf Eisen übertragen. Es entsteht Eisenoxid. Eisen wurde also oxidiert.
Homologe Reihe – Alkane, Alkene, Alkine
Alkane • Kohlenwasserstoffe, die nur Einfachbindungen enthalten, zählt man zur Stoffgruppe der Alkane.
Ihre Namen enden auf an. Manche ihrer Namen leiten sich aus dem
Griechischen je nach Anzahl der Kohlenstoff-Atome ab (z. B. penta = fünf, Pentan hat fünf Kohlenstoff-Atome).
Allgemein ist \( \text{C}_n\text{H}_{2n+2} \) die Summenformel der Alkane. Dabei steht n für die Anzahl der Kohlenstoff-Atome.
Ähnlich gebaute Stoffe, z. B. die Alkane, kann man in einer homologen Reihe anordnen. Die Formel der Alkane nimmt dabei immer um eine \( \text{CH}_2 \)-Einheit zu.
Ethan: 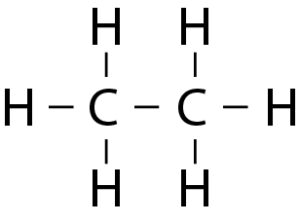
Alkene • Kohlenwasserstoffe mit einer doppelten Elektronenpaarbindung nennt man Alkene. Ihre Namen leiten sich von den Alkanen mit der Endsilbe -en ab. In der Lewis-Schreibweise wird die Doppelbindung mit einem doppelten Strich dargestellt.
Wegen der Doppelbindung besitzen Alkene grundsätzlich zwei Wasserstoff-Atome weniger als die entsprechenden Alkane.
Allgemeine Summenformel der Alkene: \( \text{C}_n\text{H}_{2n} \)
Ethen: 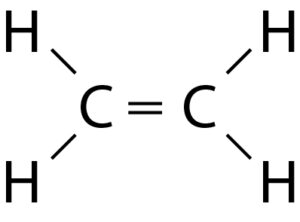
Alkine • Ein Kohlenstoff-Atom kann sogar bis zu drei Elektronenpaarbindungen zu einem anderen Kohlenstoff-Atom eingehen. Wenn eine C≡C-Dreifachbindung vorhanden ist, spricht man von einem Alkin. Die Namen der Alkine leiten sich ebenfalls von den Alkanen ab, allerdings mit der Endsilbe -in. Ihnen fehlen vier Wasserstoff-Atome im Vergleich zum Alkan.
Allgemeine Summenformel der Alkine: \( \text{C}_n\text{H}_{2n-2} \)
Ethin: ![]()
Benennung von Kohlenwasserstoffen
Dissoziieren von Säuren
Unter Dissoziieren versteht man die Auftrennung eines Moleküls in mehrere Moleküle, Atome oder Ionen.
Säuren dissoziieren (zerfallen) in Wasser in Oxonium-Ionen (\( \text{H}_3\text{O}^+ \)) und Säurerest-Ionen.
Bsp. Salzsäure:
HCl + \( \text{H}_2\text{O} \) → \( \text{H}_3\text{O}^+ \) + \( \text{Cl}^- \)
Kannst du jetzt die Aufgaben lösen? Probiere es aus
Illustrationen: Cornelsen/Detlef Seidensticker Bewegtes Bild: Cornelsen/Rainer Götze